Jena/Cottbus-Senftenberg. Die WNT-Signalübertragung ist für die Entwicklung des Organismus und die Gewebehomöostase enorm wichtig, denn die an ihr beteiligten WNT-Botenstoffe ermöglichen eine Vielzahl von Zellfunktionen. So können sie im Skelettmuskel beispielsweise die Muskelmasse erhöhen und die Regeneration verbessern. Für Therapien zur Behandlung von Erkrankungen, die mit einer verminderten Muskelmasse einhergehen z.B. Kachexie, stellt dies einen wichtigen Ansatzpunkt dar. Trotz dieser aussichtsreichen Einsatzmöglichkeiten gestaltet sich die therapeutische Anwendung bisher schwierig: Die Botenstoff-Proteine, die aus über 400 Aminosäuren bestehen, sind sehr groß und klebrig; d.h. sie verteilen sich schlecht im Gewebe, was eine medizinische Applikation erschwert. Darüber hinaus weiß man noch wenig über die funktionelle Relevanz der verschiedenen strukturellen Bereiche in den einzelnen WNT-Proteinen.
Die Forschungsgruppe „Stammzellen im Skelettmuskel“ um Prof. Julia von Maltzahn vom Leibniz-Institut für Alternsforschung - Fritz-Lipmann-Institut (FLI) in Jena und der Fakultät für Gesundheitswissenschaften der BTU Cottbus-Senftenberg in Senftenberg hat nun in einer aktuellen Studie im „Computational and Structural Biotechnology Journal“ (Open Access) herausgefunden, dass bereits ein kleiner Bestandteil des Botenstoffs WNT7A genügt, um in Muskelzellen dieselben Signalwege zu aktivieren, die der vollständige Botenstoff aktivieren kann.
Welche Bereiche sind für die WNT-Signalübertragung wichtig?
„Über die Bedeutung und funktionelle Relevanz der verschiedenen Bereiche in den WNT-Proteinen ist bisher nur recht wenig bekannt; insbesondere über die Bindestellen zum Rezeptor in den Empfängerzellen“, berichtet Prof. Julia von Maltzahn. „In unserer Studie haben wir daher speziell den C-Terminus von WNT7A untersucht, da dieser Bereich sowohl eine Haarnadel-Region (Hairpin) als auch eine Linker-Region enthält und voll funktionsfähig ist.“
Haarnadel-Region reicht aus, um Muskelwachstum zu fördern
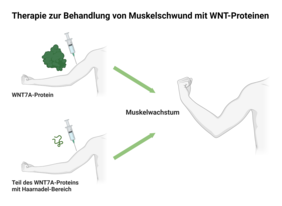
Die Forschenden fanden heraus, dass die Behandlung mit kleinen Proteinfragmenten, den C-terminalen WNT7A-Varianten, die nur die Haarnadel-Region enthalten, ausreicht, um in Muskelzellen dieselben zellulären Signalwege auszulösen, die durch das komplette WNT-Protein aktiviert werden. Der extrazelluläre Botenstoff WNT7A beeinflusst den Signalweg für das Muskelwachstum und die Erneuerung der Muskelstammzellen. Dadurch wird das Wachstum der Muskelfasern angeregt und die Vermehrung und Verteilung von Muskelstammzellen im Skelettmuskel, beispielsweise nach einer Verletzung, gefördert.
Ist Muskelschwund mit Mini-Botenstoff bald therapierbar?
„Wie unsere Ergebnisse zeigen, wird mit den von uns gefundenen, nur aus einem Haarnadel-Bereich bestehenden, Mini-Botenstoffen, eine Anwendung einer WNT7A-basierten Therapie für verschiedene Muskelschwundzustände wie Krebskachexie zunehmend wahrscheinlicher", erläutert Dr. Manuel Schmidt, Postdoc in der Forschungsgruppe und Hauptautor der Publikation.
Die Jenaer Wissenschaftler hatten in vorangegangen Studien bereits gezeigt, dass WNT7A die Muskelmasse und die Teilung von Muskelstammzellen bei Mäusen erhöht, die an Kachexie leiden, einem Muskelschwundsyndrom, von dem ein großer Teil der Krebspatienten betroffen ist. Die WNT-Proteine waren daraufhin zwar als vielversprechende Kandidaten für therapeutische Interventionen zur Verbesserung von Muskelschwundkrankheiten wie Muskeldystrophie und Krebskachexie ins Visier der Forschung gerückt, konnten aber aufgrund ihrer beträchtlichen Größe und schlechten Handhabbarkeit bisher nicht als therapeutisches Mittel zum Einsatz kommen.
Vielfältige Einsatzmöglichkeiten
Die kürzere Variante des Proteins könnte dieses Problem nun lösen. Durch seine geringe Größe scheint der extrazelluläre Botenstoff WNT7A besser dazu geeignet, eine therapeutische Anwendung zu finden. Denkbare Anwendungsmöglichkeiten wären etwa eine unterstützende Therapie beim Verlust von Muskelmasse aufgrund von Krebs oder als Stimulus für die Muskelregeneration nach Operationen. Denn WNT7A führt zur Zunahme der Population von Stammzellen im Muskel und unterstützt somit die Muskelregeneration nach Verletzungen oder Operationen.
Die Arbeit wurde durch die Deutsche Forschungsgemeinschaft sowie die Stiftung Deutsche Krebshilfe gefördert und durch das Technologietransferprogramm SPARK-FLI am Institut unterstützt. Dr. Sonja Schätzlein, Leiterin von SPARK-FLI, wertet die Forschungsergebnisse als ersten Erfolg: „Ich freue mich sehr, dass durch die finanzielle Unterstützung, die Beratung und die Vermittlung von Mentoring-Partnern aus der Industrie SPARK-FLI dazu beitragen konnte, dieses Projekt einen wichtigen Schritt auf dem Weg zu einer medizinischen Therapie voranzubringen. Auf weitere Ergebnisse bin ich sehr gespannt."
Publikation
Schmidt M, Poser C, Janster C, von Maltzahn J. The hairpin region of WNT7A is sufficient for binding to the Frizzled7 receptor and to elicit signaling in myogenic cells. Computational and Structural Biotechnology Journal. 2022, 20, 6348-6359. DOI: 10.1016/j.csbj.2022.10.047.
https://www.sciencedirect.com/science/article/pii/S2001037022004949
Information zu SPARK-FLI
Das Projekt „Counteracting cancer cachexia” wurde von 2018-2020 im Rahmen von SPARK-FLI gefördert. Das interne Technologietransferprogramm SPARK-FLI hilft dabei, grundlegende wissenschaftliche Erkenntnisse aus der biomedizinischen Forschung in die Diagnostik oder medizinische Anwendung zu übertragen und stellt sicher, dass die staatlich finanzierte Forschung zu einer verbesserten Gesundheit unserer Gesellschaft beiträgt. Durch diese gezielte Förderung erhöhen sich nicht nur die Erfolgsaussichten des jeweiligen Forschungsprojektes, auch die Kosten sowie der Zeitaufwand zur Erreichung des Ziels werden gesenkt.
Kontakt
Dr. Kerstin Wagner
Presse- und Öffentlichkeitsarbeit
Tel.: 03641-656378, E-Mail: presse@~@leibniz-fli.de