Teilbereich 1: Altern von Stammzellen
Die Forschungsgruppen innerhalb des Teilbereichs 1 untersuchen die Ursachen und Folgen der Stammzellalterung. Die Forschungsarbeit erstreckt sich von Modellorganismen über genetische Mausmodelle bis hin zu Mausmodellen, die mit menschlichen Stammzellen angereichert sind.
Mit der Schließung von zwei Gruppen in 2016 ist die Stammzellforschung an Wirbellosen-Modellen im Teilbereich 1 reduziert. Das Institut geht davon aus, dass mit der Rekrutierung neuer Gruppen diese Lücke geschlossen warden kann.
Die Forschung ist durch vier Schwerpunkte definiert:
- Zellintrinsische Mechanismen, die die Funktion alternder Stamm- und Vorläuferzellen einschränken,
- Alternsbedingte Veränderungen der Stammzellnischen und des systemischen Umfelds,
- Mechanismen der klonalen Selektion und epigenetische Drifts bei der Stammzellalterung und
- Mikrobiota- und stoffwechselbedingte Beeinträchtigungen der Stammzellfunktion während des Alterns (im Zusammenhang mit dem neuen Schwerpunkt Mikrobiota und Altern, der ím Teilbereich 2 aufgebaut wird).
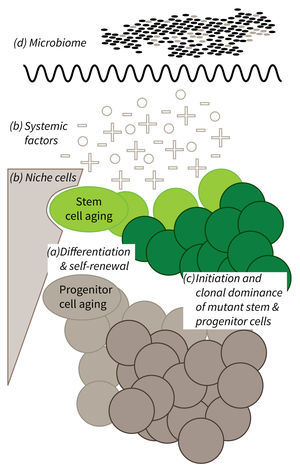
Forschungsfokus von Teilbereich 1.
a) Derzeit ist noch nicht vollständig bekannt, welche Mechanismen die Zellfunktionen im Alter beeinträchtigen. b) Der relative Einfluss von Nischenzellen und systemisch wirkenden Faktoren auf die Stammzellalterung müssen für verschiedene Gewebe noch erforscht werden. c) Die klonale Ausbreitung mutanter Zellen wird mit der Entstehung von Krankheiten im Alter in Verbindung gebracht. Mechanistisch ist der Prozess jedoch noch kaum verstanden. Die Veränderungen in der Farbintensität stehen für die klonale Dominanz von ursprünglichen Stamm- (grün) und Vorläuferzellen (grau). d) Es gibt zunehmend Hinweise darauf, dass alternsbedingte Veränderungen im Mikrobiom die Stammzellfunktion beeinflussen und vice versa.
Publikationen
(seit 2016)
2022
- Muscle stem cell maintenance and regeneration of skeletal muscle require functional motor innervation
Henze H
Dissertation 2022, Jena, Germany - Taz protects hematopoietic stem cells from an aging-dependent decrease in PU.1 activity.
Kim* KM, Mura-Meszaros* A, Tollot* M, Krishnan MS, Gründl M, Neubert L, Groth M, Rodriguez-Fraticelli A, Svendsen AF, Campaner S, Andreas N, Kamradt T, Hoffmann S, Camargo FD, Heidel FH, Bystrykh LV, de Haan G, von Eyss B
Nat Commun 2022, 13(1), 5187 * equal contribution - Meeting Report: Aging Research and Drug Discovery
Meron E, Thaysen M, Angeli S, Antebi A, Barzilai N, Baur JA, Bekker-Jensen S, Birkisdottir M, Bischof E, Bruening J, Brunet A, Buchwalter A, Cabreiro F, Cai S, Chen BH, Ermolaeva M, Ewald Collin Y, Ferrucci L, Florian MC, Fortney K, Freund A, Georgievskaya A, Gladyshev VN, Glass D, Golato T, Gorbunova V, Hoejimakers J, Houtkooper RH, Jager S, Jaksch F, Janssens G, Borch Jensen M, Kaeberlein M, Karsenty G, de Keizer P, Kennedy B, Kirkland JL, Kjaer M, Kroemer G, Lee KF, Lemaitre JM, Liaskos D, Longo VD, Lu YX, MacArthur MR, Maier AB, Manakanatas C, Mitchell SJ, Moskalev A, Niedernhofer L, Ozerov I, Partridge L, Passegué E, Petr MA, Peyer J, Radenkovic D, Rando TA, Rattan S, Riedel CG, Rudolph L, Ai R, Serrano M, Schumacher B, Sinclair DA, Smith R, Suh Y, Taub P, Trapp A, Trendelenburg AU, Valenzano DR, Verburgh K, Verdin E, Vijg J, Westendorp RGJ, Zonari A, Bakula D, Zhavoronkov A, Scheibye-Knudsen M
Aging (Albany NY) 2022, 14(2), 530–543 - Characterization of Novel α-Mangostin and Paeonol Derivatives With Cancer-Selective Cytotoxicity.
Nunna S, Huang YP, Rasa M, Krepelova A, Annunziata F, Adam L, Käppel S, Hsu MH, Neri F
Mol Cancer Ther 2022, 21(2), 257-70 - Peripheral blasts are associated with responses to ruxolitinib and outcomes in patients with chronic-phase myelofibrosis.
Palandri F, Bartoletti D, Iurlo A, Bonifacio M, Abruzzese E, Caocci G, Elli EM, Auteri G, Tiribelli M, Polverelli N, Miglino M, Heidel FH, Tieghi A, Benevolo G, Beggiato E, Fava C, Cavazzini F, Pugliese N, Binotto G, Bosi C, Martino B, Crugnola M, Ottaviani E, Micucci G, Trawinska MM, Cuneo A, Bocchia M, Krampera M, Pane F, Lemoli RM, Cilloni D, Vianelli N, Cavo M, Palumbo GA, Breccia M
Cancer 2022, 128(13), 2449-54 - YBX1 mediates translation of oncogenic transcripts to control cell competition in AML.
Perner F, Schnoeder TM, Xiong Y, Jayavelu AK, Mashamba N, Santamaria NT, Huber N, Todorova K, Hatton C, Perner B, Eifert T, Murphy C, Hartmann M, Hoell JI, Schröder N, Brandt S, Hochhaus A, Mertens PR, Mann M, Armstrong SA, Mandinova A, Heidel FH
Leukemia 2022, 36(2), 426-37 - Inflammaging is driven by upregulation of innate immune receptors and systemic interferon signaling and is ameliorated by dietary restriction.
Rasa* SMM, Annunziata* F, Krepelova A, Nunna S, Omrani O, Gebert N, Adam L, Käppel S, Höhn S, Donati G, Jurkowski TP, Rudolph KL, Ori A, Neri F
Cell Rep 2022, 39(13), 111017 * equal contribution - The hairpin region of WNT7A is sufficient for binding to the Frizzled7 receptor and to elicit signaling in myogenic cells
Schmidt M, Poser C, Janster C, von Maltzahn J
Comput Struct Biotechnol J 2022, 20, 6348-59 - Association of Telomere Length With Risk of Disease and Mortality.
Schneider CV, Schneider KM, Teumer A, Rudolph KL, Hartmann D, Rader DJ, Strnad P
JAMA INTERN MED 2022, 182(3), 291-300 - PLCG1 is required for AML1-ETO leukemia stem cell self-renewal.
Schnoeder TM, Schwarzer A, Jayavelu AK, Hsu CJ, Kirkpatrick J, Döhner K, Perner F, Eifert T, Huber N, Arreba-Tutusaus P, Dolnik A, Assi SA, Nafria M, Jiang L, Dai YT, Chen Z, Chen SJ, Kellaway SG, Ptasinska A, Ng ES, Stanley EG, Elefanty AG, Buschbeck M, Bierhoff H, Brodt S, Matziolis G, Fischer KD, Hochhaus A, Chen CW, Heidenreich O, Mann M, Lane SW, Bullinger L, Ori A, Eyss Bv, Bonifer C, Heidel F
Blood 2022, 139(7), 1080-97